Introduktion af magnesiumfluorid MgF2
Magnesiumfluorid er en uorganisk forbindelse med formlen MgF2. Forbindelsen er et hvidt krystallinsk salt og er gennemsigtigt over en bred vifte af bølgelængder, med kommercielle anvendelser i optik, der også bruges i rumteleskoper.
Magnesium (atomsymbol: Mg, atomnummer: 12) er et blok S, gruppe 2, periode 3 grundstof med en atommasse på 24,3050. Antallet af elektroner i hver af Magnesiums skaller er [2, 8, 2], og dens elektronkonfiguration er [Ne] 3s2. Magnesiumatomet har en radius på 160 pm og en Van der Waals-radius på 173 pm. Magnesium blev opdaget af Joseph Black i 1775 og først isoleret af Sir Humphrey Davy i 1808. Magnesium er det ottende mest udbredte grundstof i jordskorpen og det fjerde mest almindelige grundstof i jorden som helhed. Elementært magnesium I sin elementære form har magnesium et skinnende gråt metallisk udseende og er ekstremt reaktivt. Det kan findes i mineraler som brucit, karnallit, dolomit, magnesit, olivin og talkum. Kommercielt, magnesium bruges primært til at skabe stærke og lette aluminium-magnesium-legeringer, som har adskillige fordele i industrielle applikationer. Navnet"Magnesium"stammer fra et græsk distrikt i Thessalien kaldet Magnesia.
Fluor er et blok P, gruppe 17, periode 2-element. Dens elektronkonfiguration er [He]2s22p5. Fluoratomet har en kovalent radius på 64 pm og dets Van der Waals-radius er 135 pm. I sin elementære form, CAS 7782-41-4, har fluorgas et svagt gult udseende. Fluor blev opdaget af André-Marie Ampère i 1810. Det blev først isoleret af Henri Moissan i 1886.
Magnesiumfluorid er meget uopløseligt i vand (0,0076 g/100 ml) ved 18°C [151]. Det kan agglomereres med vand, presses til grønne pellets, afvandes og sintres ved høje temperaturer for at producere porøse pellets, der kan bruges til selektivt at fange technetium. Fanget technetium kan ikke let desorberes fra MgF2, hvilket kræver temperaturer over 1000°C. Fanget technetium kan dog nemt fjernes ved at vaske med vand eller fortyndet salpetersyre. Magnesiumfluoridet kan genbruges efter et tørretrin [152]. Magnesiumfluorid er blevet brugt i stor skala til selektiv indfangning af flygtige technetiumfluorider og oxyfluorider af technetium blandet med UF6 [22.152.153].
Magnesiumfluorid (MgF2)-holdige belægninger blev fremstillet på biologisk nedbrydelige Mg-baserede metaller gennem flussyre-involverende kemisk omdannelse (Chiu, Wong, Cheng, & Man, 2007; Lin, Tan, Wan et al., 2013; Pereda et al. , 2010; Thomann et al., 2010; Yan et al., 2010) eller MAO (Pan, Chen, Wang, & Lin, 2013; Pan, Chen, Wang, & Zhao, 2013; Seyfoori, Mirdamadi, Khavandi, & Raufi , 2012) metoder. Fluor (F) er en naturlig komponent i menneskelige knogler og tænder (Zheng, Wu, Ng, Wang, & Lian, 2002). En korrekt frigivelse af F vil ikke forårsage skade på organismerne (Thomann et al., 2010). Knogleresponsen på fluor er dosisafhængig: en lavdosis frigivelse af F vil lette knogledannelsen; dog vil en høj dosis af det forårsage dannelse af dårligt mineraliseret osteoid (Ellingsen, 1995). MgF2 er således et acceptabelt belægningsmateriale,
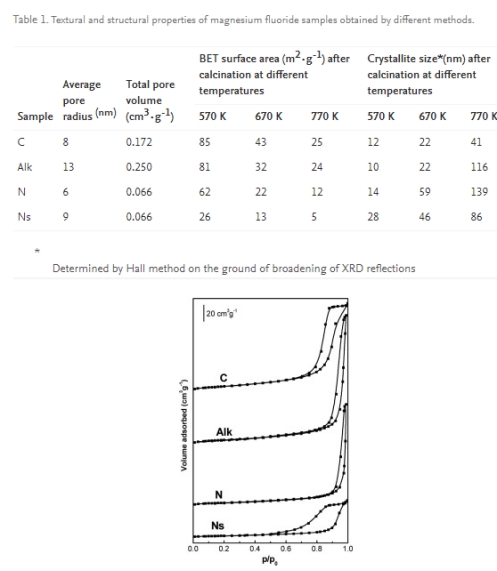
Magnesiumfluorid blev fremstillet ved hjælp af fire forskellige metoder, dog var termisk behandling af alle prøver identisk og bestod i kalcinering ved 670 K. På trods af den samme kalcineringstemperatur adskiller MgF2-prøver sig betydeligt i deres porøse struktur, hvilket afspejles i formen af hysterese-sløjfe i isotermen for lavtemperatur nitrogenadsorption, specifikt overfladeareal, porestørrelse og porevolumen (tabel 1; figur 1). Det største areal (43 m2·g-1) blev opnået i tilfælde af carbonatprøve (C), mens den mindste (13 m2)·g-1) i tilfælde af sfærisk MgF2 fremstillet af magnesiumnitrat (Ns). Adsorptions-desorptionsisotermer af alle prøver er af type IV, men de adskiller sig i formen af deres hysterese-løkker. Sidstnævnte tilhører type H1 for prøverne C, Alk og N, hvilket indikerer tilstedeværelsen af cylindriske porer, hvorimod hysteresesløjfe i prøven Ns kombinerer træk ved hystereseløkker af type H1 og H2, som man støder på, når der er smalhalsede porer til stede. Den største porestørrelse (r = 13 nm) og porevolumen (0,250 cm3)·g-1) blev fundet i magnesiumfluorid fremstillet af magnesiumalkoxid (Alk). Den diskuterede prøve er også kendetegnet ved den laveste termiske stabilitet som konkluderet af en betydelig stigning i krystallitstørrelse og drastisk reduktion i overfladeareal med stigningen i kalcineringstemperaturen (tabel 1). Den højeste modstand mod sintring og omkrystallisation ved høje temperaturer blev vist ved carbonat (C) og nitrat-sfæriske (Ns) prøver.
En del af indholdet i denne artikel kommer fra Science Direct:https://www.sciencedirect.com
FOSHAN NANHAI SHUANGFU CHEMICAL CO., LTD er en af fremstillingen afmedium og højkvalitetMagnesiumfluorid,forsyning på lang sigt produktion og levering af dette produkt over hele verden.
Attn:Nicole Huang (salgschef)
Tilføje: Qishan Industry Park, Yanfeng Road, Shishan, Nanhai-distriktet, Foshan City, Kina.
Telefon:86 757 81108788
Mobil: 86 13928083637
OG-post: sales@df-chemicals.com




